L’été arrive (si, si !). On a souvent besoin de rafraîchir rapidement et efficacement des bouteilles, pour un apéro imprévu ou un pic-nique.
Il existe quelques gestes simples pour profiter au maximum de vos glaçons !
La version courte
Pour bien rafraîchir une bouteille, il faut qu’elle soit immergée dans de l’eau froide. C’est plus efficace qu’un seau rempli seulement de glaçons.
Comptez environ 1 volume de glaçons pour 2 volumes d’eau. Et pour une eau encore plus froide, salez là (entre 50g et 100g de sel par litre d’eau)
Pour produire des glaçons plus rapidement, mettez de l’eau chaude dans votre bac à glaçons!
En cas d’urgence, vous pouvez aussi mettre les glaçons directement dans votre verre. Si vous les enlevez au bout de quelques minutes, ils auront rafraichi votre boisson sans la diluer.
Que nous dit la science ?
Chauffer ou refroidir, c’est échanger de l’énergie
Dans un corps chaud, les molécules sont agitées (pensez à l’eau qui bout ou à la vapeur d’eau). Dans un corps froid, elles le sont moins (pensez à la glace). Et les molécules n’ont qu’une idée dans la vie, c’est s’agiter !
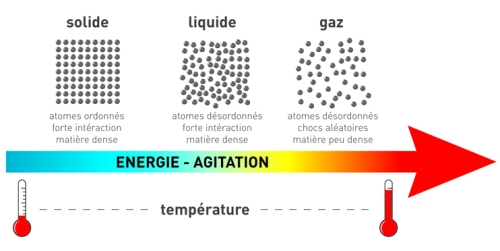
Lorsque deux corps sont en contact, le corps le plus froid va « voler » de l’énergie (sous forme de chaleur) au corps le plus chaud.

A l’équilibre, l’agitation des molécules est la même partout, et les températures des deux corps sont identiques.
L’air refroidit moins que l’eau
Quand vous mettez la main dans un four chauffé à 100°C, vous ne vous brûlez pas. Mais si vous touchez le plat, ou que vous plongez un doigt dans de l’eau bouillante, aie aie aie, ça brûle !
Pourquoi ? parce que l’air a une capacité thermique beaucoup plus faible que l’eau (3 fois moins) ou que le métal du plat.
Pour faire simple, la capacité thermique d’un corps c’est la capacité qu’il a à absorber ou à transmettre de l’énergie (un peu comme une éponge qui absorbe ou rejette plus ou moins de liquide).
Quand vous mettez votre main (ou votre doigt) dans le four ou dans l’eau à 100°C, votre main (à 37°C) « vole » de l’énergie (de la chaleur) à l’air du four ou à l’eau de la casserole : 22 kWh pour le four contre 50 kWh pour l’eau !

Pour un même volume (autour de votre main), l’air transmet 3 fois moins d’énergie (sous forme de chaleur) que l’eau : c’est pour cela que l’air est un bon isolant (double vitrage) et que l’eau est un bon fluide conducteur (chauffage des radiateurs).
C’est pour cette raison qu’il ne faut pas garder des vêtements humides quand il fait froid : ils vous volent toute votre chaleur !
Et c’est pour la même raison qu’à température égale, on ressent plus la chaleur dans une atmosphère humide (tropicale) que sèche : l’humidité dans l’air tropical vous transmet plus d’énergie que l’air sec, et vous avez plus chaud, alors que la température est la même !

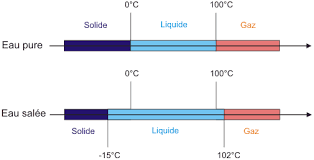
A 0°C, l’eau est à la fois solide et liquide
Pendant le réchauffement d’un glaçon, il arrive un moment où l’eau passe de l’état solide (glaçon) à l’état liquide en restant à la même température : c’est la température de fusion (0°C pour de l’eau pure à pression normale).

Vous pouvez donc mettre plein de glaçons dans votre verre de rosé (ou même de champagne) pour le rafraîchir. Ils ne le dilueront pas … à condition de les enlever au bout de quelques minutes (2 à 3 mn) !
Comment les glaçons refroidissent-ils un liquide ?
Je me suis amusé l’autre jour à poser la question à mes enfants : « pourquoi les glaçons refroidissent-ils le liquide dans lequel on les met ? ».

Une réponse a été « parce que le froid du glaçon se répand dans le verre ». Un peu comme du sirop de menthe qui se répand quand on le verse dans un verre d’eau.
Une autre réponse a été « parce que le glaçon fond et donne de l’eau froide, qui rafraîchit le liquide, comme le mitigeur du lavabo » (en fait, je crois pas qu’elle ait dit « mitigeur » mais plutôt « truc » ; mais bon, c’est l’idée qui compte !)
Et vous, qu’auriez-vous répondu ?
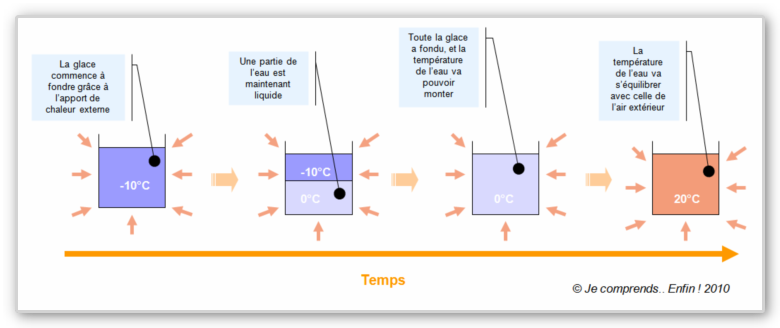
En fait, c’est un peu des deux. Quand on met un glaçon dans un liquide, le glaçon « vole » de l’énergie au liquide – et le refroidit donc – en 3 étapes :
- Dans un premier temps, le glaçon (qui est à une température négative, disons -18°C s’il sort du congélateur) va voler de l’énergie au liquide plus chaud pour casser le bel ordonnancement des molécules d’eau dans la glace. Le glaçon refroidit donc jusqu’à 0°C, mais reste sous forme de glace.
- Ensuite, la glace vole de l’énergie au liquide pour fondre (passer de l’état solide à l’état liquide) et devenir de l’eau liquide à 0°C.
- Enfin, si le liquide à refroidir est toujours à une température supérieure à 0°C, les 2 liquides se mélangent pour atteindre l’équilibre de température.
Le sel permet d’avoir une eau liquide en dessous de 0°C !
C’est le principe du salage des routes en hiver, des produits anti-gel, ou de la vodka qui ne gèle pas au congélateur.
Dans un mélange d’eau avec n’importe quel autre soluté (sel pour les routes, éthylène glycol pour les antigels de voiture, ou éthanol pour la vodka), la présence de ces solutés va gêner l’ordonnancement des molécules d’eau.
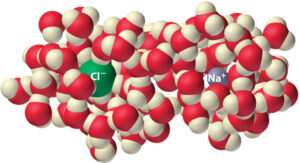
Les molécules d’eau salée vont donc avoir besoin de plus d’énergie pour se lier et se solidifier en glace que de l’eau pure.
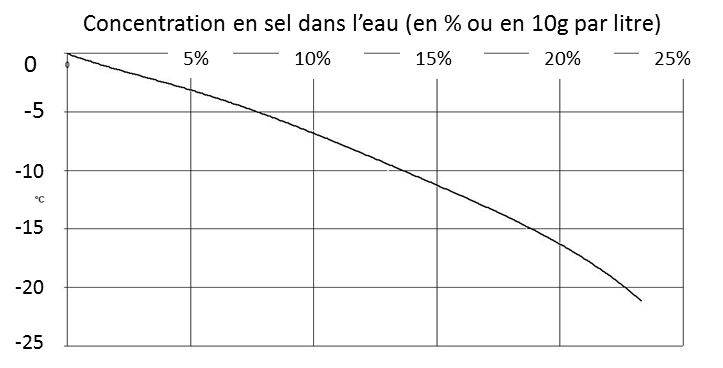
Il faut cependant de grandes quantités de sel pour avoir un effet notable : il faut par exemple une concentration de 8% (80g de sel par litre d’eau, soit 5 cuillères à soupe) pour avoir de l’eau liquide à -5°C.
Ci-joint un lien vers une vidéo amusante qui montre comment, avec un mélange d’eau salée et de glace, on peut rafraîchir une canette de soda de 24°C à 5°C en 2 minutes !
La glace conduit moins bien la chaleur que l’eau
La glace a une capacité thermique inférieure de moitié à celle de l’eau liquide. Ça veut dire qu’une quantité de glace volera 2 fois moins d’énergie que la même quantité d’eau.

C’est intéressant pour les Esquimaux, car c’est ce qui explique pourquoi les igloos sont si isolants (et en plus, la neige est constituée de 89% d’air qui est un excellent isolant thermique).
Mais c’est embêtant pour refroidir notre bouteille de rosée uniquement avec des glaçons. On va donc la plonger dans un mélange d’eau et de glaçons !
L’eau chaude gèle plus vite que l’eau froide
C’est l’effet Mpemba (du nom d’un chercheur Tanzanien – Erasto Mpemba – qui était encore élève du secondaire quand il a observé que du lait chaud mis au congélateur se transformait plus rapidement en crème glacée que la même préparation déjà froide).
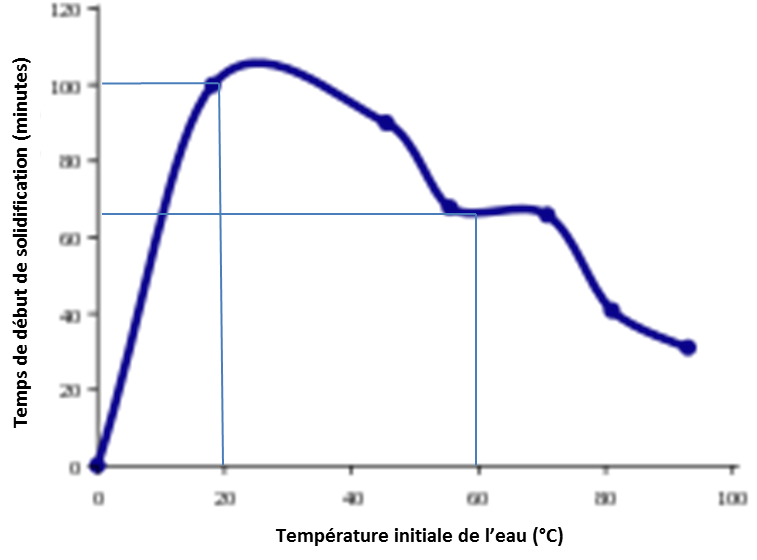
C’est pour les mêmes raisons qu’on recommande de ne pas dégivrer un pare-brise avec de l’eau chaude … ni de faire pipi dans une serrure gelée !
Quelles implications en cuisine ?
Pour refroidir une bouteille, il faut qu’elle soit dans de l’eau !
Le seau à champagne remplit de glaçons, c’est joli, mais pas efficace !
En effet, non seulement les glaçons ont une capacité thermique 2 fois moins importante que l’eau liquide, mais en plus ils ne sont pas en contact avec toute la bouteille (glaçons cubiques, bouteille ronde). Du coup, les échanges de chaleur entre la bouteille (chaude) et les glaçons (froids) ne se font pas bien.
Et même si vous utilisez de la glace pilée (pour améliorer le contact), elle rafraîchira moins la bouteille que le même volume d’eau glacée.

Il est beaucoup plus efficace de refroidir une bouteille en l’immergeant dans un seau contenant de l’eau et des glaçons : les glaçons vont refroidir l’eau, et l’eau va refroidir la bouteille en lui « volant » de l’énergie.

Un linge humide pour le congélateur
Si vous mettez une bouteille au congélateur, enveloppez-là d’un torchon humide ou de papier absorbant humide : l’eau sera en contact avec la bouteille et la rafraîchira plus et plus vite que l’air froid du congélateur !
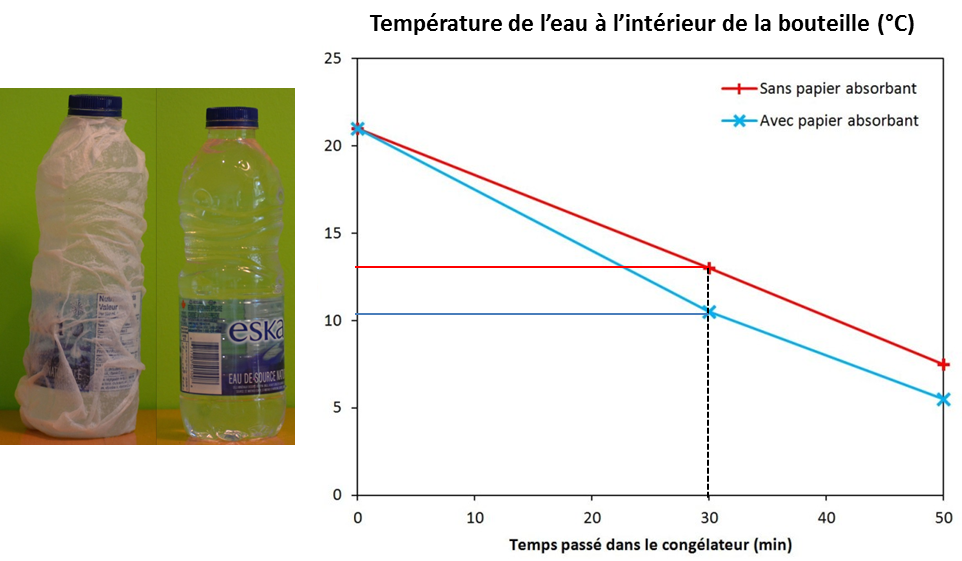
au bout de 30 minutes, la bouteille entourée d’un papier humide a perdu 4 degrés de plus (source: 3). Ça compte pour le champagne ou le rosé !
1 volume de glaçons pour 2 volumes d’eau !
Pour refroidir 1L d’eau du robinet de 22° à 0°C, il faut environ 300g de glace. Pour ceux que ça intéresse, le détail des calculs est présenté à la fin de l’article.
Mais comme votre seau à glace (ou votre bassine, ou votre poubelle) n’est pas isolant, prévoyez plutôt la moitié du volume d’eau en glace : 1 volume de glaçons pour 2 volumes d’eau.
Toute la glace ne fondra pas tout de suite, et gardera plus longtemps l’eau dans le seau à 0°C.
Pour faire des glaçons plus vite, mettez de l’eau chaude !
Pas besoin non plus de faire bouillir de l’eau, il ne faut pas exagérer ! Mais de l’eau chaude du robinet vous donnera des glaçons plus rapidement que de l’eau froide (30 minutes de gagnées quand même; quand il fait chaud, ça compte !)
En combien de temps ma bouteille va-t-elle refroidir ?
Pour répondre à cette question, c’est super compliqué ! Il faut faire appel à des tas d’équations. Je n’ai pas trouver d’explication ni de formule simple. Si quelqu’un a une formule simple à proposer, je suis preneur (utilisez les commentaires !).
J’ai trouvé un site qui propose un modèle de calcul. Si ça vous intéresse, voici le lien.
Retenez juste qu’il faut environ 10 minutes pour faire passer la température d’une bouteille de 25 degrés à 10 degrés, si elle est plongée dans un seau avec assez de glace et d’eau pour que l’ensemble reste à 0°C.
Les références
Les documents suivants m’ont aidé à préparer cet article. Que leurs auteurs en soient remerciés.
- Voyages au cœur de la science : du sel pour refroidir
- Centre de vulgarisation de la connaissance
- Scilabus: l’effet Mpemba
- Wikipedia: effet Mpemba; glace
détails des formules pour le calcul de la quantité de glaçons nécessaire pour refroidir 1L d’eau



merci Céline !
moi, c'est la "mécanique" des glaçons que je ne connaissais pas. Merci et bravo aussi !
De l'eau chaude pour des glaçons plus rapides !!! Il fallait que je lise ce billet pour l'apprendre.
Merci ! et bravo